解析基因體三維立體結構對癌細胞轉型的影響力 研究成果已刊登於Genome Biology
癌細胞的轉移是現今癌症治療最具挑戰性的課題,若能提早預測腫瘤是否有轉移的可能性,就能更精準且及時針對患者進行治療與防範。臺大醫學系黃韻如教授團隊歷時5年研究,從基因體結構出發,利用「高維度捕獲染色質構象技術」(Hi-C),發現基因體在癌細胞潛移過程中的多元機制,藉由觀察其變化,開拓另一個預測癌症轉移的新思維。這項研究突破過去研究試圖以特定基因的表現來預測癌細胞的轉移,但傳統上單一判斷的方式卻常遇到見樹不見林的困境,或是無法靈活應對腫瘤常有的個體差異性問題。此一嶄新的研究結果可望提升癌症及時的診斷與治療效率,全文已發表於國際知名期刊《基因體生物學》Genome Biology。
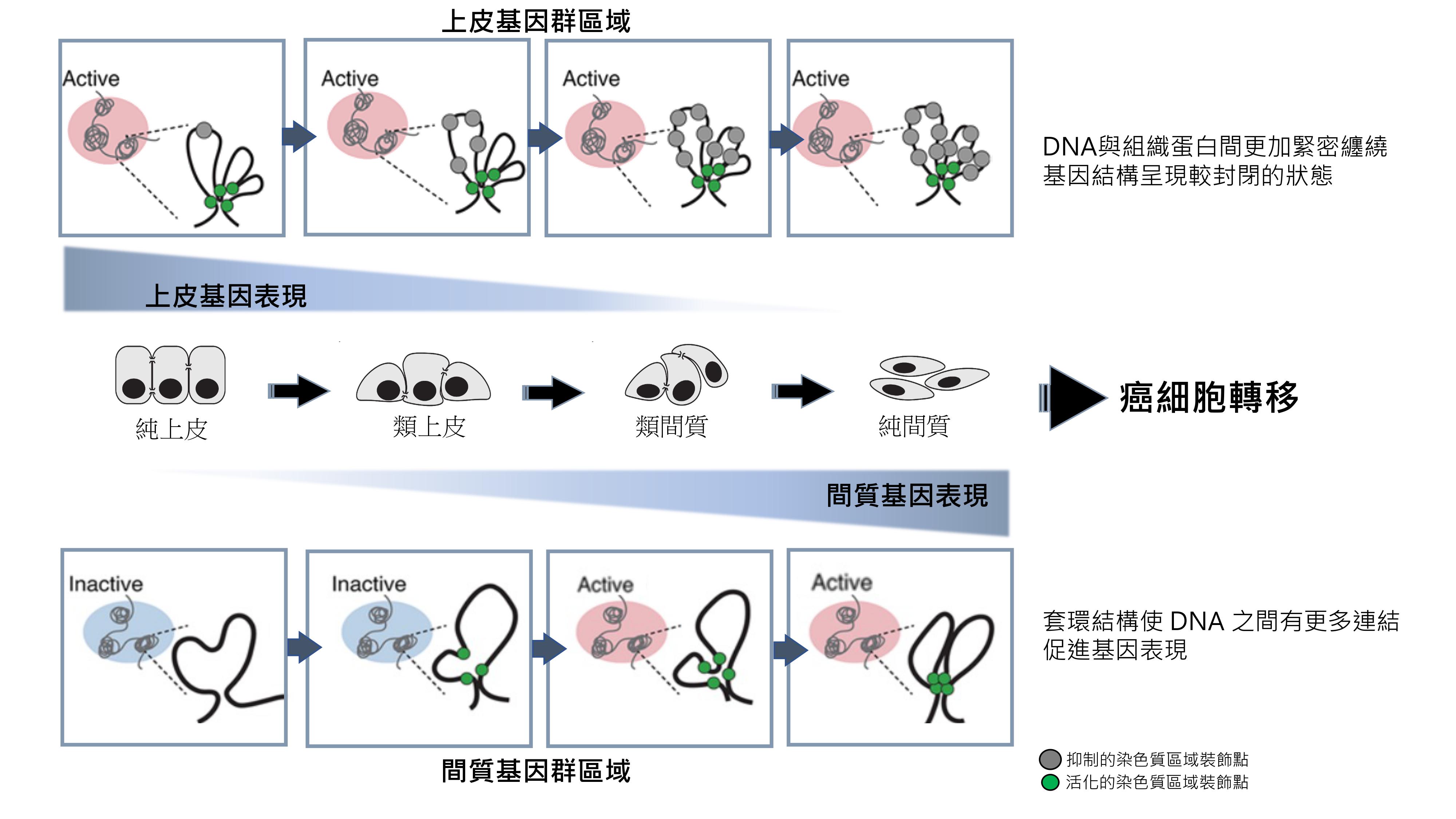
當癌細胞準備轉移時,會產生上皮—間質細胞轉型(epithelial-mesenchymal transition,EMT),由排列緊密、不易移動的上皮型癌細胞轉化成間質型癌細胞,細胞的排列會轉為鬆散且利於細胞爬行。過程中,「純上皮」細胞會先降低上皮型基因(epithelial gene)表現,形成稍不緊密「類上皮」細胞;再進一步便促進間質基因(mesenchymal gene)表現,細胞轉而形成爬行能力較強的「類間質」細胞,藉此逐步提升細胞侵襲周邊組織的能力,達到癌症轉移的目的。過去研究認為,抑制並促進特定基因的表現是在某時間點同時發生,細胞便從上皮型直接轉化成間質型,但黃教授研究團隊透過了解染色質的結構差異,發現上皮與間質基因的表現程度,是利用截然不同的調控規則及機轉來改變染色體所達成的。
此研究成果的一大突破,是透過Hi-C捕獲技術,從解析基因體的三維立體結構展現DNA的摺疊藝術。其中較沒有轉移能力的「純上皮」癌細胞要擺脫原先的上皮特徵、關閉上皮基因表現時,會針對基因的局部區塊拉起封鎖線,關起上皮分化的那道門,但不改變基因體大環境的結構;若要再進一步開啟間質基因表現,則是先將基因整體的結構舒展,讓偌大的DNA更容易遇見彼此,打開環境內互動的窗,最終成為具有高侵襲及轉移能力的「純間質」癌細胞。研究揭露出癌細胞為了轉型,在上皮基因精雕細琢,而在間質基因大刀闊斧的奧秘。
黃教授研究團隊利用特殊技術,首次開發出單細胞Hi-C的方法,並藉此觀察癌細胞的異質性,單就分析第二號或第十號染色體的立體結構變化,就足以初步預測是否具有易轉移特性的癌細胞,判斷腫瘤是否容易產生遠端轉移。
此重大發現不僅成功開創一條新途徑來破譯EMT調控背後的複雜性,更提供未來從基因結構預測腫瘤發展的新方向,進而提升癌症及時的診斷與治療效率。
本研究成果已於2022年5月30日發表於Genome Biology:
https://reurl.cc/anprml